【飛諾美色譜】封面故事專題 | ADC藥物的液相色譜-質譜分析解決方案
抗體偶聯藥物(ADC)是一種將小分子細胞毒素藥物通過連接子與單克隆抗體偶聯形成的藥物。與傳統的小分子化學治療以及抗腫瘤單抗相比,ADC藥物不僅可以提高化學治療的療效和腫瘤細胞的特異性,還可以降低或減弱系統毒性以及非靶向細胞毒性。ADC結構復雜,異質性高,存在多種產品相關的雜質,其理化性質分析與結構表征不僅包括單抗部分,還包括小分子藥物相關的質量屬性,可見ADC的質量屬性研究較抗體更為復雜。本期#封面故事我們將圍繞藥物抗體比(Drug-to-antibody ratio, DAR)關鍵質量屬性,闡述ADC藥物的質量分析與控制的進展與綜合分析方案。

ADC藥物經過90多年的發展,特別是近來20多年的高速發展,目前經過定點偶聯技術是第三代ADC藥物成功開發的關鍵。小分子毒素與單克隆抗體的位點特異性結合確保ADC藥物具有明確、均一的DAR值(通常為2或4),這樣可以使藥物毒性降低,穩定性和藥代動力學顯著提高。第三代ADC藥物采用的位點特異性偶聯技術主要包括Thiomab、ThioBridge、引入非天然氨基酸、引入序列標簽或聚糖等。

藥物抗體比(Drug-to-antibody ratio, DAR)指抗體偶聯上毒素小分子數量的平均值,直接反映了靶向腫瘤細胞的載荷數量,同時影響藥物的安全性與有效性。如下圖 所示,DAR的分析方法主要分為二類:
A. 液相色譜法(HPLC-UV)
B. 質譜法(LC-MS)
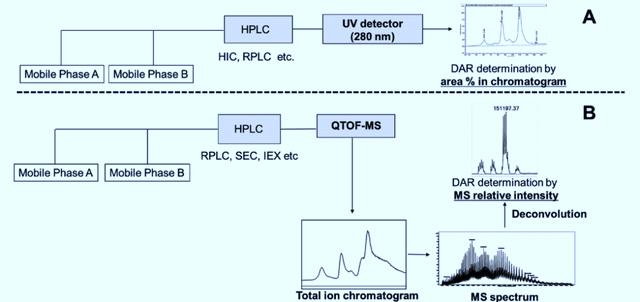
液相色譜法(HPLC-UV)
1) HIC-UV分析法:
疏水作用色譜(HIC-HPLC)是根據抗體偶聯不同數量的細胞毒性小分子之間疏水性不同,也即是具有不同DAR的ADC分子可在HIC中實現分離,未偶聯小分子藥物的抗體疏水性最弱,優先被洗脫,偶聯小分子藥物數量越多的抗體,其疏水性就越強,典型譜圖見下圖 。

HIC-UV分析mAb與ADC譜圖
HIC是在非變性條件下進行的,不僅可以用于不同DAR分子的分離,還可以用于純化,進一步對分離純化后的HIC各組分進行深度研究。
一般情況下,半胱氨酸的偶聯方式之一,是將抗體部分還原,打開鏈間二硫鍵,游離半胱氨酸上的巰基(-SH)與毒素小分子-連接子上的馬來酰亞胺基團反應形成DAR=0-8分子異質體ADC。依據計算公式DAR=∑(Weighted Peak Area)/100,最終得到加權平均DAR=3.6。
2) RPLC-UV方法:
反相高效液相色譜法(RP-HPLC)通常是在還原水平上分析DAR,即通過非變性還原條件下打開鏈間二硫鍵,然后根據待測物質的極性大小進行分離,具有更好的分離度與分辨率。理論上基于半胱氨酸偶聯方式ADC經過還原前處理后得到6種亞基分子類型,分別是L0、L1、H0、H1、H2與H3,見下圖所示:

基于半胱氨酸偶聯方式ADC的還原前處理
這里我們可以看到通過連接物與MMAF偶聯的曲妥珠單抗的DAR。該抗體通過部分還原使鏈間二硫鍵變為半胱氨酸殘基,之后該殘基再與小分子藥物通過連接物形成一種藥物抗體偶聯物。在此色譜圖中,我們可以觀察到重鏈和輕鏈,連接有小分子藥物或者沒有連接小分子藥物片段,分別用H0-H3和L0/L1來表示。DAR通過將H0-H3, L0和L1的峰面積相加來確定,并決定它們對mAb的貢獻,然后再取平均值。

曲妥珠單抗Mc-MMAF半胱氨酸偶聯物的平均DAR
色譜柱:bioZen Intact XB-C8,3.6μm
貨號:00F-4766-AN
規格:150x2.1mm
流動相A:0.1%TFA水溶液
流動相B:0.1%TFA in ACN
流速:0.4mL/min
檢測:LC-UV(280nm)
樣品:曲妥單抗mcMMAF半胱氨酸偶聯物(來源于ADC BiotechnologyLTD)
儀器:UPLC-UV
這里,我們采用了Phenomenex的bioZen Intact XB-C8色譜柱,此款色譜柱是core-shell結構,類似于經典的Kinetex系列:

對于ADC的Dar值分析,具有以下優點:
• 優化的顆粒形態可實現更高效率的Intact RP
• 改善蛋白質回收率
• 高溫穩定性<90°C
以相同的分析方式,我們可以將標準子單元的分析平臺化,同時,也可以將具有不同linker的ADC平臺化。這樣可以加快分析速度。

色譜柱:bioZen3.6μmXB-C8
貨號:00F-4766-AN
規格:150x2.1mm
流動相A:0.1%TFA in 水
流動相B:0.1%TFA in 乙腈
流速:0.4mL/min
梯度:
28-34%B in 1-4minutes
34-65%B in 4-10minutes
檢測器:UV-Vis,280nm
溫度:80°
樣品:如圖所示
隨著越來越多的研究者采用特定位點的偶聯技術來提高治療效果和降低毒性,ADC的同質化程度將會越來越高,DAR的分析也將變得更加簡單。但是,隨著新型細胞毒素和連接物以及偶聯方法的增加,有效載荷復雜性不斷增加,這一趨勢將使DAR測定更多地轉向LC-MS技術,以利用其高分辨率分析能力。
質譜法(LC-MS)
質譜法可分為變性與非變性電噴霧質譜法,兩種不同的方法均是根據物質的分子量差異進行DAR的分析。抗體偶聯上不同數量細胞毒性小分子后,ADC呈現分子異質性,不同的DAR物質在高分辨質譜的分析下具有不同的質荷比(m/z),然后根據相對應的DAR質譜信號峰強度或峰面積計算平均DAR值。
1) 變性質譜法(Denatured MS)
通常情況下,DAR在變性質譜分析中,會使用到有機試劑流動相與相對較高的柱溫,ADC在這兩種條件的共同作用下,非共價鍵連接的空間結構被破壞,然后經過電噴霧攜帶相對較多的電荷(H+),進而產生信噪比(S/N)較好的質譜峰圖。
變性質譜常應用于ADC賴氨酸偶聯方式的DAR分析,因其分子異質性較高,往往在進行質譜分析之前,需要對其進行去糖基化處理或者使用CPB酶去除C端賴氨酸的影響,以減少圖譜的復雜程度,便于后續的峰歸屬及最終的平均DAR計算。

Kadcyla ADC與生物類似藥ADC的去糖基化
2) 非變性質譜法(Native MS)
非變性質譜使用與質譜兼容的流動相體系,以及相對較低的柱溫與更溫和的電離方式,在不破壞物質非共價鍵連接的立體空間結構情況下,讓ADC生物大分子在氣相中保持自然折疊狀態,既可以用于ADC鏈間半胱氨酸偶聯方式的DAR分析,也可以用于賴氨酸偶聯方式的DAR分析。
HIC-MS非變性質譜可與HIC-HPLC質量放行方法相結合用于DAR的分析與質控,具有高效率與高通量等特點。
SEC-MS非變性質譜也常用于ADC DAR的分析與質控。相對HIC-MS來說,流動相可選擇揮發性的鹽溶液,與質譜更兼容些。
我們分析了從Sigma購得的市售半胱氨酸連接的ADC 模擬物,使用bioZen SEC-2與SCIEX® X500B聯用鑒定DAR 0到8。根據提取離子色譜圖,每種藥物抗體蛋白型都用于計算DAR。平均DAR計算為3.4,與Sigma報告值4.0±0.8匹配。我們看到在“天然”條件下,ADC保持完整,從而可以觀察到不同的DAR種類,并且可以標記DAR和糖型。

LC Conditions
Column:bioZen 1.8μm SEC-2
Dimension:150x4.6mm
Part No.:00F-4769-E0
Recommended Guard:SecurityGuard™ ULTRA
Guard Cartridge Part No.:AJ0-9850
Guard Holder Part No.:AJ0-9000
Mobile Phase:100mM Ammonium Acetate
Flow Rate:200μL/min
Temperature:25℃
Detector:QTOF(SCIEX X500B)
Sample:Sigma ADC Mimic(MSQC8),100μg
這里我們用到了bioZen 1.8µm dSEC色譜柱,這款色譜柱的特點一是采用了低孔隙體積的硅膠,實現更好的穩定性和重現性。二是采用了親水性二醇類鍵合表面,能夠防止硅膠表面與蛋白質樣品相互作用。

比如我們還可以見到很多高分辨質譜上的應用:
Intact Mass:Cysteine-based conjugation (DAR)

同時,對于半胱氨酸偶聯的ADC藥物,可以采用非變性的模式進行分子量的檢測,從而分析DAR值。

半胱氨酸偶聯的ADC藥物質譜檢測圖譜
對于ADC藥物的開發而言,如何依據藥物的偶聯方式及目標屬性去選擇合適的質量控制方法、質量控制項目與性質合適的耗材,是助力藥物從理論設計走向實驗室制備的重要環節。本文總結的幾種ADC藥物DAR值分析方法,不僅能給用戶提供不同的選擇,還能幫助用戶進行不同方法的相互驗證,確保結果的準確性。
后面我們會繼續跟蹤行業的進展,給大家最及時的技術交流和分享。更多內容,詳見《2023飛諾美色譜產品指南》

《下載2023飛諾美色譜產品指南》
免責聲明
- 凡本網注明“來源:化工儀器網”的所有作品,均為浙江興旺寶明通網絡有限公司-化工儀器網合法擁有版權或有權使用的作品,未經本網授權不得轉載、摘編或利用其它方式使用上述作品。已經本網授權使用作品的,應在授權范圍內使用,并注明“來源:化工儀器網”。違反上述聲明者,本網將追究其相關法律責任。
- 本網轉載并注明自其他來源(非化工儀器網)的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品第一來源,并自負版權等法律責任。
- 如涉及作品內容、版權等問題,請在作品發表之日起一周內與本網聯系,否則視為放棄相關權利。
 手機版
手機版 化工儀器網手機版
化工儀器網手機版
 化工儀器網小程序
化工儀器網小程序
 官方微信
官方微信 公眾號:chem17
公眾號:chem17
 掃碼關注視頻號
掃碼關注視頻號


















 采購中心
采購中心